Электрический ток в жидкостях. Движение зарядов, анионы катионы
Жидкости, как и любые другие вещества, могут быть проводниками, полупроводниками и диэлектриками. Например, дистиллированная вода будет являться диэлектриком, а растворы и расплавы электролитов будут являться проводниками. Полупроводниками будут являться, например, расплавленный селен или расплавы сульфидов.
Ионная проводимость
Электролитическая диссоциация - это процесс распадения молекул электролитов на ионы под действием электрического поля полярных молекул воды. Степенью диссоциации называется доля молекул распавшихся на ионы в растворенном веществе.
Степень диссоциации будет зависеть от различных факторов: температура, концентрация раствора, свойства растворителя. При увеличении температуры, степень диссоциации тоже будет увеличиваться.
После того как молекулы разделились на ионы, они движутся хаотично. При этом два иона разных знаков могут рекомбинироваться, то есть снова объединиться в нейтральные молекулы. При отсутствии внешних изменений в растворе должно установиться динамическое равновесие. При нем число молекул которое распалось на ионы за единицу времени, будет равняться числу молекул, которые снова объединятся.
Носителями зарядов в водных растворах и расплавах электролитов будут являться ионы. Если сосуд с раствором или расплавом включить в цепь, то положительно заряженные ионы начнут двигаться к катоду, а отрицательные – к аноду. В результате этого движения возникнет электрический ток. Данный вид проводимости называют ионной проводимостью.
Помимо ионной проводимости в жидкостях может обладать и электронной проводимостью. Такой тип проводимости свойственен, например, жидким металлам. Как отмечалось выше, при ионной проводимости прохождение тока связано с переносом вещества.
Электролиз
Вещества которые входят в состав электролитов, будут оседать на электродах. Этот процесс называется в электролизом. Электролиз – процесс выделения на электроде вещества, связанный с окислительно-восстановительными реакциями.
Электролиз нашел широкое применение в физике и технике. С помощью электролиза поверхность одного металла покрывают тонким слоем другого металла. Например, хромирование и никелирование.
С помощью электролиза можно получить копию с рельефной поверхности. Для этого необходимо, чтобы слой металла, который осядет на поверхности электрода, легко можно было снять. Для этого иногда на поверхность наносят графит.
Процесс получения таких легко отслаиваемых покрытий получил название гальвано-пластика. Этим метод разработал русский ученый Борис Якоби при изготовлении полых фигур для Исаакиевского собора с Санкт-Петербурге.
>>Физика: Электрический ток в жидкостях
Жидкости, как и твердые тела, могут быть диэлектриками, проводниками и полупроводниками. К числу диэлектриков относится дистиллированная вода, к проводникам - растворы и расплавы электролитов: кислот, щелочей и солей. Жидкими полупроводниками являются расплавленный селен, расплавы сульфидов и др.
Электролитическая диссоциация.
При растворении электролитов под влиянием электрического поля полярных молекул воды происходит распад молекул электролитов на ионы. Этот процесс называется электролитической диссоциацией
.
Степень диссоциации
, т. е. доля в растворенном веществе молекул, распавшихся на ионы, зависит от температуры, концентрации раствора и электрических свойств растворителя. С увеличением температуры степень диссоциации возрастает и, следовательно, увеличивается концентрация положительно и отрицательно заряженных ионов.
Ионы разных знаков при встрече могут снова объединиться в нейтральные молекулы - рекомбинироватъ
. При неизменных условиях в растворе устанавливается динамическое равновесие, при котором число молекул, распадающихся за секунду на ионы, равно числу пар ионов, которые за то же время вновь объединяются в нейтральные молекулы.
Ионная проводимость.
Носителями заряда в водных растворах или расплавах электролитов являются положительно и отрицательно заряженные ионы.
Если сосуд с раствором электролита включить в электрическую цепь, то отрицательные ионы начнут двигаться к положительному электроду - аноду, а положительные - к отрицательному - катоду. В результате установится электрический ток. Поскольку перенос заряда в водных растворах или расплавах электролитов осуществляется ионами, такую проводимость называют ионной
.
Жидкости могут обладать и электронной проводимостью . Такой проводимостью обладают, например, жидкие металлы.
Электролиз.
При ионной проводимости прохождение тока связано с переносом вещества. На электродах происходит выделение веществ, входящих в состав электролитов. На аноде отрицательно заряженные ионы отдают свои лишние электроны (в химии это называется окислительной реакцией), а на катоде положительные ионы получают недостающие электроны (восстановительная реакция). Процесс выделения на электроде вещества, связанный с окислительно-восстановительными реакциями, называют электролизом
.
Применение электролиза.
Электролиз широко применяют в технике для различных целей. Электролитическим путем покрывают поверхность одного металла тонким слоем другого (никелирование, хромирование, омеднение
и т. п.). Это прочное покрытие защищает поверхность от коррозии.
Если обеспечить хорошее отслаивание электролитического покрытия от поверхности, на которую осаждается металл (этого достигают, например, нанося на поверхность графит), то можно получить копию с рельефной поверхности.
В полиграфической промышленности такие копии (стереотипы) получают с матриц (оттиск набора на пластичном материале), для чего осаждают на матрицах толстый слой железа или другого вещества. Это позволяет воспроизвести набор в нужном количестве экземпляров. Если раньше тираж книги ограничивался числом оттисков, которые можно получить с одного набора (при печатании набор постепенно стирается), то сейчас использование стереотипов позволяет значительно увеличить тираж. Правда, в настоящее время с помощью электролиза получают стереотипы только для книг высококачественной печати.
Процесс получения отслаиваемых покрытий - гальванопластика
- был разработан русским ученым Б. С. Якоби (1801-1874), который в 1836 г. применил этот способ для изготовления полых фигур для Исаакиевского собора в Санкт-Петербурге.
При помощи электролиза осуществляют очистку металлов от примесей. Так, полученную из руды неочищенную медь отливают в форме толстых листов, которые затем помещают в ванну в качестве анодов. При электролизе медь анода растворяется, примеси, содержащие ценные и редкие металлы, выпадают на дно, а на катоде оседает чистая медь.
При помощи электролиза получают алюминий из расплава бокситов. Именно этот способ получения алюминия сделал его дешевым и наряду с железом самым распространенным в технике и быту.
С помощью электролиза получают электронные платы, служащие основой всех электронных изделий. На диэлектрик наклеивают тонкую медную пластину, на которую наносят особой краской сложную картину соединяющих проводов. Затем пластину помещают в электролит, где вытравливаются незакрытые краской участки медного слоя. После этого краска смывается и на плате появляются детали микросхемы.
В растворах и расплавах электролитов свободные электрические заряды появляются за счет распада на ионы нейтральных молекул. Движение ионов в поле означает перенос вещества. Этот процесс широко используется на практике (электролиз).
???
1. Что называют электролитической диссоциацией?
2. Почему при прохождении тока по раствору электролита происходит перенос вещества, а при прохождении по металлическому проводнику перенос вещества не происходит?
3. В чем состоит сходство и различие собственной проводимости у полупроводников и у растворов электролитов?
Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс
Скачать календарно-тематическое планирование по физике , ответы на тесты, задания и ответы школьнику, книги и учебники , курсы учителю по физике для 10 класса
Содержание урока конспект урока опорный каркас презентация урока акселеративные методы интерактивные технологии Практика задачи и упражнения самопроверка практикумы, тренинги, кейсы, квесты домашние задания дискуссионные вопросы риторические вопросы от учеников Иллюстрации аудио-, видеоклипы и мультимедиа фотографии, картинки графики, таблицы, схемы юмор, анекдоты, приколы, комиксы притчи, поговорки, кроссворды, цитаты Дополнения рефераты статьи фишки для любознательных шпаргалки учебники основные и дополнительные словарь терминов прочие Совершенствование учебников и уроков исправление ошибок в учебнике обновление фрагмента в учебнике элементы новаторства на уроке замена устаревших знаний новыми Только для учителей идеальные уроки календарный план на год методические рекомендации программы обсуждения Интегрированные урокиЕсли у вас есть исправления или предложения к данному уроку,
То, что жидкости могут отлично проводить электрическую энергию, знают абсолютно все. И также общеизвестным фактом является то, что все проводники по своему типу делятся на несколько подгрупп. Предлагаем рассмотреть в нашей статье, как электрический ток в жидкостях, металлах и прочих полупроводниках проводится, а также законы электролиза и его виды.
Теория электролиза
Чтобы было легче понять, о чем идет речь, предлагаем начать с теории, электричество, если мы рассматриваем электрический заряд, как своего рода жидкость, стало известным уже более 200 лет. Заряды состоят из отдельных электронов, но те, настолько малы, что любой большой заряд ведет себя как непрерывного течения, жидкость.
Как и тела твердого типа, жидкие проводники могут быть трех типов:
- полупроводниками (селен, сульфиды и прочие);
- диэлектиками (щелочные растворы, соли и кислоты);
- проводниками (скажем, в плазме).
Процесс, при котором происходит растворение электролитов и распадение ионов под воздействием электрического молярного поля, называется диссоциация. В свою очередь, доля молекул, которые распались на ионы, либо распавшихся ионов в растворенном веществе, полностью зависит от физических свойств и температуры в различных проводниках и расплавах. Обязательно нужно помнить, что ионы могут рекомбинироваться или вновь объединиться. Если условия не будут меняться, то количество распавшихся ионов и объединившихся будет равно пропорциональным.
В электролитах проводят энергию ионы, т.к. они могут являться и положительно заряженными частицами, и отрицательно. Во время подключения жидкости (или точнее, сосуда с жидкостью к сети питания), начнется движение частиц к противоположным зарядам (положительные ионы начнут притягиваться к катодам, а отрицательные – к анодам). В этом случае, энергию транспортируют непосредственно, ионы, поэтому проводимость такого типа называется – ионной.
Во время этого типа проводимости, ток переносят ионы, и на электродах выделяются вещества, которые являются составляющими электролитов. Если рассуждать с точки зрения химии, то происходит окисление и восстановление. Таким образом, электрический ток в газах и жидкостях транспортируется при помощи электролиза.
Законы физики и ток в жидкостях
Электричество в наших домах и технике, как правило, не передается в металлических проволоках,. В металле электроны могут переходить от атома к атому, и, таким образом нести отрицательный заряд.
Как жидкости, они приводятся в виде электрического напряжения, известного как напряжение, изменяемом в единицах – вольт, в честь итальянского ученого Алессандро Вольта.
Видео: Электрический ток в жидкостях: полная теория
Также, электрический ток течет от высокого напряжения в низкое напряжение и измеряется в единицах, известных как ампер, названных по имени Андре-Мари Ампера. И согласно теории и формулы, если увеличить напряжение тока, то его сила также увеличится пропорционально. Это соотношение известно как закон Ома. Как пример, виртуальная ампермерная характеристика ниже.
Рисунок: зависимость тока от напряженияЗакон Ома (с дополнительными подробностями относительно длины и толщины проволоки), как правило, является одним из первых вещей, преподаваемых в классах, изучающих физику, многие студенты и преподаватели поэтому рассматривают электрический ток в газах и жидкостях как основной закон в физике.
Для того чтобы увидеть своими глазами движение зарядов, нужно приготовить колбу с соленой водой, плоские прямоугольные электроды и источники питания, также понадобится ампермерная установка, при помощи которой будет проводиться энергия от сети питания к электродам.
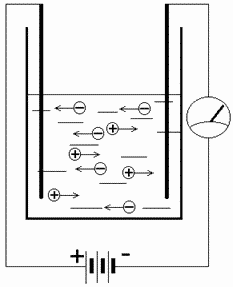 Рисунок: Ток и соль
Рисунок: Ток и соль
Пластины, которые выступают проводниками необходимо опустить в жидкость, и включить напряжение. После этого начнется хаотичное перемещение частиц, но как после возникновения магнитного поля между проводниками, этот процесс упорядочится.
Как только ионы начнут меняться зарядами и объединяться, аноды станут катодами, а катоды – анодами. Но здесь нужно учитывать и электрическое сопротивление. Конечно, не последнюю роль играет теоретическая кривая, но основное влияние – это температура и уровень диссоциации (зависит от того, какие носители будут выбраны), а также выбран переменный ток или постоянный. Завершая это опытное исследование, Вы можете обратить внимание, что на твердых телах (металлических пластинах), образовался тончайший слой соли.
Электролиз и вакуум
Электрический ток в вакууме и жидкостях – это достаточно сложный вопрос. Дело в том, что в таких средах полностью отсутствуют заряды в телах, а значит, это диэлектрик. Иными словами, наша цель – это создание условий, для того, чтобы атом электрона мог начать свое движение.
Для того нужно использовать модульное устройство, проводники и металлические пластины, а далее действовать, как и в методе выше.
 Проводники и вакуум
Проводники и вакуум
 Характеристика тока в вакууме
Характеристика тока в вакууме
Применение электролиза
Этот процесс применяется практически во всех сферах жизни. Даже самые элементарные работы подчас требуют вмешательства электрического тока в жидкостях, скажем,
При помощи этого простого процесса происходит покрытие твердых тел тончайшим слоем какого-либо металла, например, никелирование иди хромирование Т.е. это один из возможных способов борьбы с коррозийными процессами. Подобные технологии используются в изготовлении трансформаторов, счетчиков и прочих электрических приборов.
Надеемся, наше обоснование ответило на все вопросы, которые возникают, изучая явление электрический ток в жидкостях. Если нужны более качественные ответы, то советуем посетить форум электриков, там Вас с радостью проконсультируют бесплатно.
Практически каждому человеку известно определение электрического тока как Однако все дело в том, что происхождение и движение его в различных средах достаточно сильно отличается друг от друга. В частности, электрический ток в жидкостях обладает несколько другими свойствами, чем Речь идет о тех же металлических проводниках.
Основное отличие состоит в том, что ток в жидкостях - это движение заряженных ионов, то есть атомов или даже молекул, которые по какой-либо причине потеряли или приобрели электроны. При этом одним из показателей этого движения является изменение свойств того вещества, по которому данные ионы проходят. Опираясь на определение электрического тока, мы можем предположить, что при разложении отрицательно заряженные ионы будут двигаться в сторону положительного а положительные, наоборот, к отрицательному.
Процесс разложения молекул раствора на положительные и отрицательные заряженные ионы получил в науке название электролитической диссоциации. Таким образом, электрический ток в жидкостях возникает вследствие того, что, в отличие от того же металлического проводника, изменяется состав и химические свойства этих жидкостей, результатом чего является процесс перемещения заряженных ионов.
Электрический ток в жидкостях, его происхождение, количественные и качественные характеристики были одной из главных проблем, изучением которой долгое время занимался знаменитый физик М. Фарадей. В частности, с помощью многочисленных экспериментов ему удалось доказать, что масса выделяемого при электролизе вещества напрямую зависит от количества электричества и времени, в течении которого этот электролиз осуществлялся. Ни от каких других причин, за исключением рода вещества, эта масса не зависит.
Кроме того, изучая ток в жидкостях, Фарадей экспериментально выяснил, что для выделения одного килограмма любого вещества при электролизе необходимо одно и то же количество Это количество, равное 9,65.10 7 к., получило название числа Фарадея.
В отличие от металлических проводников, электрический ток в жидкостях оказывается окруженным которые значительно затрудняют передвижение ионов вещества. В связи с этим, в любом электролите возможно образование тока только небольшого напряжения. В то же время, если температура раствора повышается, то его проводимость увеличивается, а поля возрастает.
Электролиз обладает еще одним интересным свойством. Все дело в том, что вероятность распада той или иной молекулы на положительные и отрицательные заряженные ионы тем выше, чем большее число молекул собственно вещества и растворителя. В то же время, в определенный момент наступает перенасыщение раствора ионами, после чего проводимость раствора начинает снижаться. Таким образом, наиболее сильная будет проходить в растворе, где концентрация ионов крайне невелика, однако напряженность электрического тока в таких растворах будет крайне низкой.
Процесс электролиза нашел широкое применение в различных промышленных производствах, связанных с проведением электрохимических реакций. К числу наиболее важных из них можно отнести получение металла с помощью электролитов, электролиз солей, содержащих хлор и его производные, окислительно-восстановительные реакции, получение такого необходимого вещества, как водород, полировка поверхностей, гальваника. Например, на многих предприятиях машино- и приборостроения весьма распространен метод рафинирования, который представляет собой получение металла без всяких ненужных примесей.
К жидкостям, являющимся проводниками, относятся расплавы и растворы электролитов, т.е. солей, кислот и щелочей.
При растворении электролитов в воде происходит распад их молекул на ионы – электролитическая диссоциация. Степень диссоциации, т.е. доля в растворенном веществе молекул, распавшихся на ионы, зависит от температуры, концентрации раствора и электрических свойств растворителя. С увеличением температуры степень диссоциации возрастает и, следовательно, увеличивается концентрация положительно и отрицательно заряженных ионов. Ионы разных знаков при встрече могу снова объединиться в нейтральные молекулы. Такой процесс называется рекомбинация. При неизменных условиях в растворе устанавливается динамическое равновесие, при котором число молекул, распадающихся за секунду на ионы, равно числу пар ионов, которые за то же время вновь объединяются в нейтральные молекулы.
Т.о., свободными носителями зарядов в проводящих жидкостях являются положительные и отрицательные ионы. Если в жидкость поместить электроды подключенные к источнику тока, то эти ионы начнут придут в движение. Один из электродов подключен к отрицательному полюсу источника тока – он называется катод – другой подключен к положительному - анод. При подключении к источнику тока ионы в растворе электролита отрицательные ионы начинают двигаться к положительному электроду (аноду), а положительные – соответственно к отрицательному (катоду). То есть установится электрический ток. Такую проводимость в жидкостях называют ионной, так как носителями заряда являются ионы.
При прохождении тока через раствор электролита на электродах происходит выделение вещества, связанное с окислительно-восстановительными реакциями. На аноде отрицательно заряженные ионы отдают свои лишние электроны (окислительная реакция), а на катоде положительные ионы принимают недостающие электроны (восстановительная реакция). Такой процесс называется электролизом.
При электролизе на электродах происходит выделение вещества. Зависимость массы выделившегося вещества m от силы тока, времени прохождения тока и самого вещества установил М.Фарадей. Этот закон можно получить теоретически. Итак, масса выделившегося вещества равна произведению массы одного иона m i на число ионов N i , достигших электрода за время Dt. Масса иона согласно формуле количества вещества равна m i =M/N a , где M – молярная масса вещества, N a – постоянная Авогадро. Число ионов, достигших электрода, равно N i =Dq/q i , где Dq – заряд, прошедший электролит за время Dt (Dq=I*Dt), q i – заряд иона, который определяется валентностью атома (q i = n*e, где n – валентность атома, e – элементарный заряд). При подстановке этих формул получаем, что m=M/(neN a)*IDt. Если обозначить через k (коэффициент пропорциональности) =M/(neN a), то имеем m=kIDt. Это математическая запись первого закона Фарадея – одного из законов электролиза. Масса вещества, выделившегося на электроде за время Dt при прохождении электрического тока, пропорциональна силе тока и этому промежутку времени. Величину k называют электрохимическим эквивалентом данного вещества, который численно равен массе вещества, выделившегося на электродах, при переносе ионами заряда, равного 1 Кл. [k]= 1 кг/Кл. k = M/(neN a) = 1/F*M/n , где F – постоянная Фарадея. F=eN a =9,65*10 4 Кл/моль. Выведенная формула k=(1/F)*(M/n) является вторым законом Фарадея.
Электролиз широко применяется в технике для различных целей, например,так покрывают поверхность одного металла тонким слоем другого (никелирование, хромирование, омеднение и др.). Если обеспечить хорошее отслаивание электролитического покрытия от поверхности, то можно получить копию рельефа поверхности. Этот процесс называется гальванопластика. Также при помощи электролиза осуществляют очистку металлов от примесей, например, толстые листы неочищенной меди, полученной из руды, помещают в ванну в качестве анода. В процессе электролиза медь растворяется, примеси выпадают на дно, а на катоде оседает чистая медь. С помощью электролиза ещё получают электронные платы. На диэлектрик наклеивают тонкую сложную картину соединяющих проводов, затем помещают пластину в электролит, где вытравливаются незакрытые краской участки медного слоя. После этого краска смывается и на плате появляются детали микросхемы.